Los anticuerpos, también conocidos como inmunoglobulinas, son proteínas especializadas producidas por el sistema inmunitario para identificar y neutralizar agentes patógenos como bacterias, virus y toxinas. Estas moléculas desempeñan un papel fundamental en la defensa del organismo, actuando como soldados moleculares que reconocen sustancias extrañas llamadas antígenos y desencadenan una respuesta inmune específica para eliminarlas. En este artículo exploraremos su estructura, los diferentes tipos que existen, sus funciones y su importancia en la medicina moderna.
¿Qué son los anticuerpos?
Los anticuerpos son glucoproteínas producidas por los linfocitos B, un tipo de glóbulo blanco del sistema inmunitario adaptativo. Cuando el organismo detecta la presencia de un antígeno —cualquier sustancia que el cuerpo reconoce como extraña o potencialmente peligrosa—, los linfocitos B se activan y se transforman en células plasmáticas, las cuales secretan grandes cantidades de anticuerpos específicos contra ese antígeno.
Cada anticuerpo posee una especificidad única que le permite unirse a un antígeno determinado, de manera similar a como una llave encaja en una cerradura. Esta unión antígeno-anticuerpo es el primer paso para la eliminación del agente invasor. Los anticuerpos actúan atacando, debilitando y destruyendo los antígenos, según la información proporcionada por MedlinePlus.
El sistema inmunitario tiene la capacidad de recordar los antígenos con los que ha entrado en contacto previamente, lo que permite una respuesta más rápida y eficaz ante futuras exposiciones. Este mecanismo es la base de la inmunidad activa, que se desarrolla tras una infección o mediante la vacunación.
Estructura de los anticuerpos
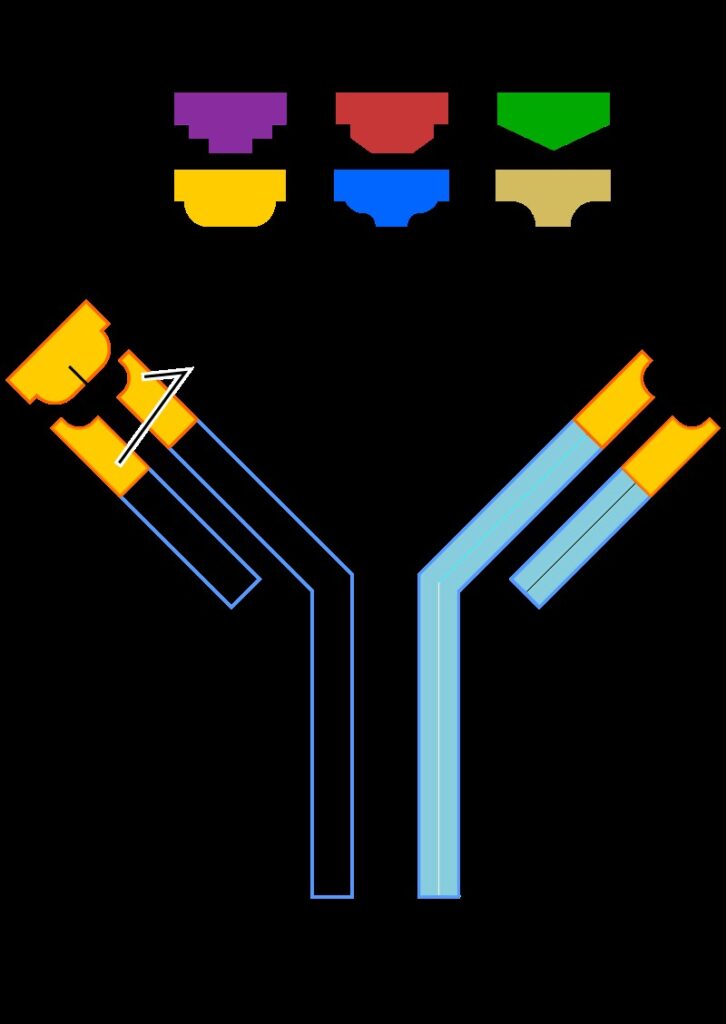
Los anticuerpos presentan una estructura característica en forma de Y, que resulta esencial para comprender su funcionamiento. Cada molécula de anticuerpo está compuesta por cuatro cadenas polipeptídicas: dos cadenas pesadas (heavy chains) idénticas y dos cadenas ligeras (light chains) idénticas, unidas entre sí por puentes disulfuro.
La estructura del anticuerpo se divide en dos regiones funcionales principales:
- Fragmento Fab (Fragment antigen-binding): Corresponde a los dos brazos superiores de la Y. Cada fragmento Fab contiene una región variable que determina la especificidad del anticuerpo, es decir, a qué antígeno puede unirse. Esta región es única para cada anticuerpo y le permite reconocer un epítopo específico del antígeno.
- Fragmento Fc (Fragment crystallizable): Es la base o tallo de la Y. Esta región es constante dentro de cada clase de inmunoglobulina y es responsable de interactuar con receptores celulares y componentes del sistema del complemento, mediando las funciones efectoras del anticuerpo.
Además, cada cadena posee una región constante y una región variable. Las regiones variables de las cadenas pesada y ligera se combinan para formar el sitio de unión al antígeno, también conocido como paratopo. La diversidad de las regiones variables permite al sistema inmunitario generar millones de anticuerpos diferentes, capaces de reconocer prácticamente cualquier antígeno.
En la zona donde los brazos de la Y se unen al tallo se encuentra la región bisagra, que confiere flexibilidad a la molécula y le permite ajustar la distancia entre los dos sitios de unión al antígeno para adaptarse a diferentes configuraciones antigénicas.
Tipos de inmunoglobulinas
Existen cinco clases principales de inmunoglobulinas en el ser humano, cada una con características estructurales y funcionales distintas:
IgG (Inmunoglobulina G)
Es el anticuerpo más abundante en la sangre y los fluidos extracelulares, representando aproximadamente el 75-80% de todos los anticuerpos séricos. La IgG es la única inmunoglobulina capaz de atravesar la placenta, proporcionando inmunidad pasiva al feto y al recién nacido durante los primeros meses de vida. Participa activamente en la neutralización de toxinas, la opsonización de patógenos y la activación del sistema del complemento.
IgA (Inmunoglobulina A)
Es el anticuerpo predominante en las secreciones mucosas, incluyendo la saliva, las lágrimas, la leche materna y las secreciones del tracto respiratorio, gastrointestinal y genitourinario. La IgA secretora actúa como primera línea de defensa en las superficies mucosas, impidiendo la adhesión de patógenos a las células epiteliales. Representa aproximadamente el 10-15% de las inmunoglobulinas séricas.
IgM (Inmunoglobulina M)
Es el primer anticuerpo producido durante la respuesta inmune primaria y el primero que sintetiza el feto. Se encuentra principalmente en el torrente sanguíneo en forma de pentámero (cinco unidades unidas), lo que le confiere 10 sitios de unión al antígeno y una gran capacidad para activar el complemento y aglutinar patógenos. Representa aproximadamente el 5-10% de las inmunoglobulinas séricas.
IgE (Inmunoglobulina E)
Aunque es la inmunoglobulina menos abundante en el suero sanguíneo, desempeña un papel crucial en las reacciones alérgicas y en la defensa contra parásitos, especialmente helmintos. La IgE se une a receptores de alta afinidad en mastocitos y basófilos; cuando el antígeno se une a la IgE fijada en estas células, se produce la liberación de histamina y otros mediadores inflamatorios responsables de los síntomas alérgicos.
IgD (Inmunoglobulina D)
Se encuentra principalmente en la superficie de los linfocitos B maduros, donde actúa como receptor de antígenos junto con la IgM. Su función exacta no está completamente esclarecida, pero se cree que participa en la activación y diferenciación de los linfocitos B. Su concentración sérica es muy baja, representando menos del 1% de las inmunoglobulinas totales.
Función de los anticuerpos
Los anticuerpos cumplen diversas funciones protectoras que son esenciales para la eliminación de agentes patógenos. Los tres mecanismos principales son:
Neutralización
Los anticuerpos pueden unirse directamente a los patógenos o a las toxinas que estos producen, bloqueando su capacidad de infectar células o causar daño. Al cubrir la superficie del agente invasor, los anticuerpos impiden que este interactúe con los receptores celulares necesarios para la infección. Este mecanismo es particularmente importante en la defensa contra virus y toxinas bacterianas.
Opsonización
Mediante la opsonización, los anticuerpos recubren la superficie del patógeno y facilitan su reconocimiento y fagocitosis por parte de células del sistema inmunitario como los macrófagos y los neutrófilos. El fragmento Fc del anticuerpo es reconocido por los receptores Fc presentes en la superficie de los fagocitos, lo que potencia significativamente la eficiencia de la fagocitosis.
Activación del complemento
Los anticuerpos, especialmente la IgM y la IgG, pueden activar la vía clásica del sistema del complemento, un conjunto de proteínas plasmáticas que actúan en cascada para destruir patógenos. La activación del complemento puede resultar en la formación del complejo de ataque a membrana (MAC), que perfora la membrana del patógeno causando su lisis, así como en la generación de moléculas que promueven la inflamación y atraen más células inmunitarias al sitio de la infección.
Además de estos tres mecanismos principales, los anticuerpos también participan en la citotoxicidad celular dependiente de anticuerpos (ADCC), donde células como los linfocitos NK reconocen el fragmento Fc de los anticuerpos unidos al patógeno y liberan sustancias citotóxicas para destruir la célula infectada.
Anticuerpos y vacunas
Las vacunas aprovechan la capacidad del sistema inmunitario para generar anticuerpos y crear memoria inmunológica. Al introducir en el organismo una versión debilitada, inactivada o fragmentada de un patógeno, las vacunas estimulan la producción de anticuerpos específicos sin causar la enfermedad.
Cuando el sistema inmunitario entra en contacto con el antígeno vacunal, se desencadena una respuesta inmune primaria que produce anticuerpos IgM inicialmente, seguidos de anticuerpos IgG más específicos y de mayor afinidad. Además, se generan linfocitos B de memoria que permanecen en el organismo durante años o incluso toda la vida.
Si la persona vacunada se expone posteriormente al patógeno real, los linfocitos B de memoria se activan rápidamente y producen grandes cantidades de anticuerpos de alta afinidad en un tiempo mucho menor que la respuesta primaria. Esta respuesta inmune secundaria es más rápida, intensa y eficaz, lo que permite neutralizar al patógeno antes de que pueda causar una enfermedad significativa.
Las vacunas han sido fundamentales en la erradicación de enfermedades como la viruela y en la reducción drástica de la incidencia de enfermedades como el sarampión, la poliomielitis y la difteria. Los diferentes tipos de vacunas incluyen vacunas de virus vivos atenuados, vacunas inactivadas, vacunas de subunidades, vacunas conjugadas y las más recientes vacunas de ARNm.
Anticuerpos monoclonales
Los anticuerpos monoclonales son anticuerpos producidos en laboratorio que se diseñan para unirse a un antígeno específico. A diferencia de los anticuerpos policlonales producidos naturalmente por el sistema inmunitario, los anticuerpos monoclonales son idénticos entre sí y reconocen exactamente el mismo epítopo del antígeno diana.
La tecnología de producción de anticuerpos monoclonales fue desarrollada en 1975 por César Milstein y Georges Köhler, quienes recibieron el Premio Nobel de Medicina en 1984 por este descubrimiento. El proceso implica la fusión de un linfocito B productor de anticuerpos con una célula de mieloma, creando un hibridoma que puede producir anticuerpos indefinidamente.
En la actualidad, los anticuerpos monoclonales tienen numerosas aplicaciones terapéuticas:
- Oncología: Anticuerpos como el trastuzumab (Herceptin) se utilizan para tratar el cáncer de mama HER2-positivo, mientras que el rituximab se emplea en el tratamiento de linfomas.
- Enfermedades autoinmunes: El adalimumab y el infliximab bloquean el factor de necrosis tumoral (TNF) y se utilizan en artritis reumatoide, enfermedad de Crohn y psoriasis.
- Enfermedades infecciosas: Se han desarrollado anticuerpos monoclonales para tratar infecciones como la COVID-19 y prevenir la infección por virus respiratorio sincitial (VRS).
- Diagnóstico médico: Los anticuerpos monoclonales son herramientas esenciales en pruebas diagnósticas como los test de embarazo, las pruebas de detección de enfermedades infecciosas y las técnicas de inmunohistoquímica.
Los anticuerpos monoclonales humanizados y completamente humanos han reducido significativamente los problemas de rechazo inmunológico asociados con los primeros anticuerpos monoclonales de origen murino, ampliando enormemente sus aplicaciones clínicas.
Los anticuerpos o inmunoglobulinas son proteínas producidas por los linfocitos B del sistema inmunitario. Su función principal es reconocer y unirse a sustancias extrañas llamadas antígenos, como bacterias, virus y toxinas, para neutralizarlas y facilitar su eliminación del organismo. Actúan como moléculas de defensa específicas que protegen al cuerpo contra infecciones y enfermedades.
En el cuerpo humano existen cinco clases principales de anticuerpos o inmunoglobulinas: IgG (la más abundante, representa el 75-80% del total), IgA (predominante en secreciones mucosas), IgM (la primera en producirse ante una infección), IgE (involucrada en reacciones alérgicas y defensa contra parásitos) e IgD (presente en la superficie de los linfocitos B maduros).
La forma de Y de los anticuerpos es funcionalmente importante. Los dos brazos superiores (fragmentos Fab) contienen las regiones variables que se unen específicamente a los antígenos, mientras que la base (fragmento Fc) interactúa con células inmunitarias y proteínas del complemento. La región bisagra entre ambas partes proporciona flexibilidad para adaptarse a diferentes antígenos.
El fragmento Fab (Fragment antigen-binding) es la parte del anticuerpo que se une directamente al antígeno y determina su especificidad. El fragmento Fc (Fragment crystallizable) es la base de la molécula que interactúa con receptores de células inmunitarias y con el sistema del complemento, mediando las funciones efectoras como la opsonización y la activación del complemento.
Las vacunas introducen una versión inofensiva del patógeno (debilitada, inactivada o fragmentada) para estimular al sistema inmunitario a producir anticuerpos específicos y linfocitos B de memoria. Si la persona se expone al patógeno real posteriormente, estos linfocitos de memoria generan una respuesta inmune secundaria más rápida y potente, produciendo anticuerpos de alta afinidad que neutralizan la infección antes de que cause enfermedad.
La opsonización es un proceso mediante el cual los anticuerpos recubren la superficie de un patógeno, marcándolo para su destrucción. Los fagocitos como los macrófagos y neutrófilos poseen receptores Fc que reconocen los anticuerpos adheridos al patógeno, lo que facilita y potencia enormemente la fagocitosis, es decir, la ingestión y destrucción del microorganismo invasor.
Los anticuerpos monoclonales son anticuerpos producidos en laboratorio diseñados para reconocer un antígeno específico. Se utilizan ampliamente en medicina para tratar diversos tipos de cáncer (como el trastuzumab para cáncer de mama), enfermedades autoinmunes (como el adalimumab para artritis reumatoide), enfermedades infecciosas y también como herramientas de diagnóstico médico en pruebas como los test de embarazo.
La IgE es la inmunoglobulina responsable de las reacciones alérgicas. Se une a receptores de alta afinidad en mastocitos y basófilos. Cuando un alérgeno (como el polen o los ácaros) se une a la IgE fijada en estas células, provoca la liberación de histamina y otros mediadores inflamatorios que causan los síntomas alérgicos típicos como estornudos, picazón, inflamación y dificultad respiratoria.
Referencias
- MedlinePlus. Sistema inmunitario y sus enfermedades. Biblioteca Nacional de Medicina de EE. UU. Disponible en: medlineplus.gov
- Abbas, A.K., Lichtman, A.H., & Pillai, S. Inmunología celular y molecular. 10.ª edición. Elsevier, 2022.
- Janeway, C.A. et al. Immunobiology: The Immune System in Health and Disease. 9th edition. Garland Science.
- Köhler, G. & Milstein, C. (1975). Continuous cultures of fused cells secreting antibody of predefined specificity. Nature, 256(5517), 495-497.