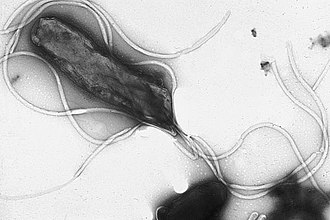
¿Qué es el Helicobacter pylori?
Cómo sobrevive en el ambiente ácido
H. pylori ha desarrollado mecanismos únicos para sobrevivir en el hostil ambiente ácido del estómago (pH 1-2). El más importante es la producción de ureasa, enzima que hidroliza la urea en amoníaco y CO₂, creando una nube alcalina alrededor de la bacteria que neutraliza el ácido localmente. Además, sus flagelos le permiten moverse en el moco gástrico y sus adhesinas le facilitan la unión al epitelio gástrico.
Consecuencias de la infección
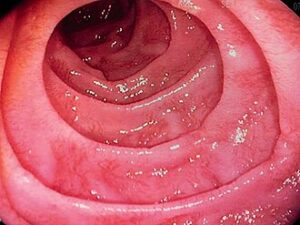
- Gastritis crónica activa: presente en prácticamente todos los infectados
- Úlcera péptica: el 15-20% de los infectados desarrollará úlcera gástrica o duodenal
- Adenocarcinoma gástrico: la IARC clasifica a H. pylori como carcinógeno del grupo 1; causa ~75% de los cánceres gástricos no cardiales
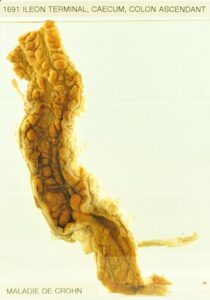
- Linfoma MALT gástrico: su erradicación puede resolver el linfoma en estadios precoces
- La mayoría de infectados (≈70-80%) permanecen asintomáticos
Diagnóstico
Las pruebas no invasivas incluyen el test del aliento con urea-13C (gold standard no invasivo), el antígeno en heces y la serología (menos útil por persistencia de anticuerpos post-erradicación). Las pruebas invasivas (endoscopia con biopsia) permiten cultivo, histología y test rápido de ureasa.
Tratamiento: erradicación antibiótica
La erradicación se basa en pautas antibióticas combinadas. La terapia cuádruple con bismuto (IBP + bismuto + tetraciclina + metronidazol, 10-14 días) es actualmente la recomendada en España por las guías del Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa (GETECCU) y el grupo de H. pylori, dado el aumento de resistencias a la claritromicina. La confirmación de erradicación se realiza 4-8 semanas después mediante test del aliento o antígeno en heces.
⚕️ Importante: No debes automedicarte con antibióticos para tratar H. pylori. El uso inadecuado genera resistencias y dificulta la erradicación. Consulta a tu médico si tienes síntomas digestivos crónicos para realizar el diagnóstico y seguir la pauta antibiótica adecuada.
Referencias
- MedlinePlus – Biblioteca Nacional de Medicina de EE.UU.
- Organización Mundial de la Salud (OMS)
- Mayo Clinic
H. pylori es una bacteria gramnegativa que coloniza la mucosa gástrica de casi la mitad de la población mundial. Produce ureasa que neutraliza el ácido estomacal permitiendo su supervivencia. Es la principal causa de gastritis crónica, úlcera péptica y el principal factor de riesgo de cáncer gástrico, clasificado como carcinógeno de grupo 1 por la IARC.
El contagio es fecal-oral (agua o alimentos contaminados) y oral-oral (saliva). Es más frecuente en condiciones de hacinamiento, saneamiento deficiente y países en desarrollo. La mayoría de las infecciones se adquieren en la infancia. La prevalencia supera el 70% en países en desarrollo frente al 30-40% en desarrollados.
Los métodos diagnósticos incluyen: test del aliento con urea marcada (no invasivo, alta sensibilidad), antígeno en heces (no invasivo), serología (detecta anticuerpos pero no distingue infección activa de pasada), biopsia gástrica endoscópica (gold standard, permite cultivo y antibiograma).
El tratamiento estándar es la terapia cuádruple: IBP (omeprazol) + bismuto + tetraciclina + metronidazol, o la terapia concomitante (IBP + amoxicilina + claritromicina + metronidazol), durante 10-14 días. La erradicación se confirma al menos 4 semanas después con test del aliento o antígeno en heces.
Las guías actuales recomiendan tratar la infección si se detecta, independientemente de los síntomas, dado su papel en la úlcera péptica, el linfoma MALT y el cáncer gástrico. La estrategia «test and treat» (buscar y erradicar en pacientes con dispepsia sin signos de alarma) es coste-efectiva.
Sí. H. pylori es el principal factor de riesgo de cáncer gástrico (adenocarcinoma). La infección crónica genera gastritis atrófica, metaplasia intestinal y displasia hasta el cáncer en un 1-3% de los infectados. La erradicación reduce el riesgo de cáncer gástrico significativamente, especialmente si se realiza antes de la aparición de lesiones premalignas.
La resistencia a la claritromicina (>15% en España) y el metronidazol es creciente y amenaza la eficacia de los esquemas clásicos. Por eso se recomienda cada vez más el cultivo y antibiograma antes de tratar, o usar regímenes cuádruples que no incluyan claritromicina en zonas de alta resistencia.
La reinfección tras erradicación exitosa es posible pero infrecuente en países desarrollados (menos del 2-3% anual). Es más frecuente en países con alta prevalencia y en niños que viven con adultos infectados. No existe vacuna disponible actualmente aunque hay varias en investigación.