¿Qué es el sistema del complemento?
El sistema del complemento es un conjunto de proteínas séricas inactivas que circulan en la sangre y los fluidos tisulares, listas para activarse ante la presencia de patógenos. Estas proteínas, denominadas con la letra C seguida de un número (C1 a C9), junto con factores como B, D y properdina, funcionan como una cascada proteolítica: la activación de una proteína desencadena la activación de la siguiente, amplificando enormemente la respuesta. Una vez activado, el complemento cumple tres funciones principales: la opsonización de microorganismos para facilitar su fagocitosis, la activación de la inflamación mediante la liberación de mediadores químicos, y la lisis directa de células invasoras a través de la formación de poros en sus membranas.
Vía clásica de activación
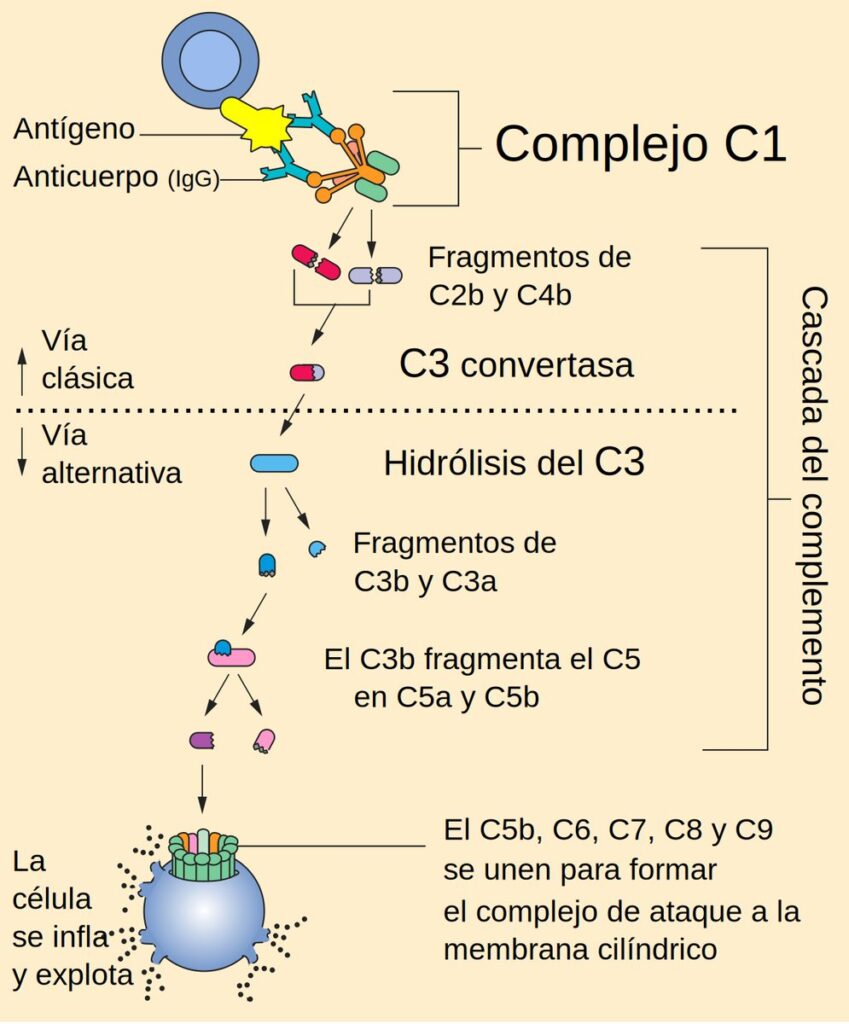
La vía clásica fue la primera en ser descubierta y constituye el puente principal entre la inmunidad adaptativa y el sistema del complemento. Se inicia cuando la proteína C1q se une a complejos antígeno-anticuerpo formados en la superficie del patógeno. La unión de C1q activa las serina proteasas C1r y C1s de forma autocatalítica, lo que desencadena una serie de reacciones en cadena:
- Activación de C1: C1q reconoce las regiones Fc de los anticuerpos IgG o IgM unidos al antígeno, lo que provoca la activación secuencial de C1r y C1s
- Escisión de C4 y C2: la proteasa C1s activa corta C4 en C4a y C4b, y C2 en C2a y C2b. El fragmento C4b se deposita sobre la superficie del patógeno
- Formación de la C3 convertasa: los fragmentos C4b y C2a se combinan para formar el complejo C4b2a, conocido como C3 convertasa de la vía clásica, capaz de escindir grandes cantidades de C3
- Amplificación: una sola C3 convertasa puede generar hasta 1000 moléculas de C3b que se depositan covalentemente sobre la superficie del patógeno
Vía alternativa de activación
La vía alternativa es filogenéticamente la más antigua y no requiere anticuerpos para su activación, por lo que funciona como un mecanismo de defensa inmediata. Se activa de forma espontánea mediante la hidrólisis continua de C3 en el plasma, un proceso conocido como «tickover»:
- Hidrólisis espontánea de C3: C3 se hidroliza espontáneamente en el plasma generando C3(H₂O), una molécula que adquiere la capacidad de unirse al factor B
- Acción del factor D: el factor D escinde al factor B unido a C3(H₂O), generando el fragmento Bb que permanece asociado formando la C3 convertasa inicial C3(H₂O)Bb
- Bucle de amplificación: el C3b generado se deposita sobre superficies cercanas y, si se trata de un patógeno, se une al factor B para formar una nueva C3 convertasa (C3bBb), estabilizada por la properdina
- Discriminación propio-extraño: las células del huésped poseen proteínas reguladoras como el factor H y DAF (CD55) que inactivan C3b, mientras que las superficies de patógenos carecen de estos reguladores, permitiendo la amplificación
Vía de las lectinas
La vía de las lectinas comparte similitudes estructurales con la vía clásica, pero se activa de manera independiente de los anticuerpos. Su activación depende del reconocimiento de patrones moleculares de carbohidratos presentes en la superficie de los patógenos:
- Lectina de unión a manosa (MBL): es una colectina similar a C1q que reconoce residuos de manosa, fucosa y N-acetilglucosamina abundantes en bacterias, hongos, virus y parásitos, pero escasos en células humanas
- Ficolinas: proteínas de reconocimiento de patrones que, al igual que la MBL, activan esta vía al unirse a carbohidratos específicos de patógenos
- Activación de MASP-1 y MASP-2: la unión de MBL o ficolinas al patógeno activa las serina proteasas asociadas a MBL (MASP-1 y MASP-2), que funcionan de forma análoga a C1r y C1s
- Convergencia con la vía clásica: MASP-2 escinde C4 y C2, generando la misma C3 convertasa C4b2a que la vía clásica
Formación del complejo de ataque a la membrana (MAC)
Las tres vías de activación convergen en la formación de la C5 convertasa, que inicia el ensamblaje del complejo de ataque a la membrana (MAC), la estructura responsable de la lisis directa de patógenos. Cuando C3b se une a la C3 convertasa existente, se forma la C5 convertasa que escinde C5 en dos fragmentos: C5a, un potente mediador inflamatorio, y C5b, que inicia la cascada terminal:
- Unión de C5b a C6: C5b se asocia con C6 formando un complejo estable en la superficie del patógeno
- Incorporación de C7: C7 se une al complejo C5b-C6 y experimenta un cambio conformacional que expone una región hidrofóbica, permitiendo su inserción parcial en la membrana lipídica
- Anclaje por C8: C8 se une al complejo y penetra profundamente en la bicapa lipídica, formando un pequeño poro inicial
- Polimerización de C9: múltiples moléculas de C9 (entre 10 y 16) se polimerizan alrededor del complejo, formando un poro transmembrana de aproximadamente 100 angstroms de diámetro
- Lisis celular: el poro permite el flujo libre de iones y agua, destruyendo el gradiente electroquímico de la célula y causando su lisis osmótica
Funciones del sistema del complemento
Opsonización
La opsonización es el proceso mediante el cual los fragmentos del complemento, especialmente C3b, iC3b y C3dg, se depositan covalentemente sobre la superficie de los patógenos, marcándolos para ser reconocidos y fagocitados por células del sistema inmunitario. Los fagocitos como los macrófagos y neutrófilos poseen receptores específicos para estos fragmentos:
- CR1 (CD35): receptor que reconoce C3b y C4b, presente en macrófagos, neutrófilos, eritrocitos y células B
- CR3 (CD11b/CD18): receptor de iC3b que puede desencadenar la fagocitosis por sí solo
- CR2 (CD21): receptor de C3dg presente en linfocitos B, que potencia la respuesta de anticuerpos
- CR4: receptor adicional que reconoce derivados inactivados de C3b
Activación de la inflamación
Los fragmentos pequeños generados durante la activación del complemento, conocidos como anafilotoxinas, son potentes mediadores de la respuesta inflamatoria. C5a es el más potente, seguido de C3a y C4a. Estas moléculas actúan sobre receptores acoplados a proteínas G en diversas células para producir:
- Aumento de la permeabilidad vascular, permitiendo la llegada de proteínas plasmáticas al sitio de infección
- Quimiotaxis de neutrófilos y monocitos hacia el foco infeccioso
- Activación de mastocitos y basófilos con liberación de histamina
- Contracción del músculo liso
- Estimulación de la producción de citocinas proinflamatorias por macrófagos
Lisis celular directa
A través de la formación del MAC, el complemento puede destruir directamente bacterias gramnegativas, células infectadas por virus y eritrocitos extraños. El poro formado por el MAC permite el flujo descontrolado de iones y agua, lo que destruye el equilibrio osmótico de la célula y provoca su muerte. Este mecanismo es particularmente importante en la defensa contra bacterias del género Neisseria, como las causantes de meningitis y gonorrea.
Regulación del sistema del complemento
Dado su enorme potencial destructivo, el sistema del complemento cuenta con múltiples mecanismos de regulación para proteger las células propias del organismo:
- Inhibidor de C1 (C1INH): serina proteasa que inactiva C1r y C1s, previniendo la activación descontrolada de la vía clásica. Su deficiencia causa el angioedema hereditario
- Factor H: proteína reguladora que se une preferentemente a C3b depositado sobre células propias gracias a su afinidad por el ácido siálico, promoviendo la inactivación de C3b por el factor I
- Factor I: serina proteasa que degrada C3b y C4b con ayuda de cofactores, impidiendo la formación de convertasas
- DAF (CD55): proteína de membrana que acelera la disociación de las C3 y C5 convertasas en la superficie de células propias
- MCP (CD46): cofactor de membrana que facilita la inactivación de C3b y C4b por el factor I
- CD59 (protectina): proteína de membrana que impide la inserción de C9 y la formación del MAC en células propias
Importancia clínica
Las deficiencias en los componentes del complemento se asocian con diversas enfermedades:
- Deficiencia de C3: aumenta enormemente la susceptibilidad a infecciones bacterianas graves y recurrentes
- Deficiencia de componentes terminales (C5-C9): predispone específicamente a infecciones por bacterias del género Neisseria
- Deficiencia de C1INH: causa angioedema hereditario con episodios de edema grave
- Deficiencia de MBL: aumenta las infecciones en la primera infancia, antes de la maduración de la inmunidad adaptativa
- Mutaciones en CD59 y DAF: causan hemoglobinuria paroxística nocturna, con destrucción de glóbulos rojos propios
- Activación excesiva: contribuye a enfermedades autoinmunes como el lupus eritematoso sistémico y la glomerulonefritis
Preguntas frecuentes
El sistema del complemento es un conjunto de más de 30 proteínas plasmáticas y de membrana que actúan en cascada para defender al organismo contra patógenos. Recibe su nombre porque fue descubierto como un factor del suero sanguíneo que complementaba la acción de los anticuerpos en la destrucción de bacterias. Forma parte esencial tanto de la inmunidad innata como de la adaptativa.
Las tres vías son la vía clásica, que se activa por complejos antígeno-anticuerpo mediante la proteína C1q; la vía alternativa, que se activa espontáneamente por hidrólisis de C3 y no requiere anticuerpos; y la vía de las lectinas, que se activa cuando la lectina de unión a manosa (MBL) reconoce carbohidratos en la superficie de patógenos. Las tres vías convergen en la formación de C3 convertasa y la activación de la cascada terminal.
El complejo de ataque a la membrana (MAC) es una estructura formada por las proteínas C5b, C6, C7, C8 y múltiples moléculas de C9 que se ensamblan en la membrana del patógeno. Este complejo forma un poro transmembrana de aproximadamente 100 angstroms de diámetro que permite el flujo libre de iones y agua, destruyendo el equilibrio osmótico de la célula invasora y provocando su lisis. Es el mecanismo final de destrucción directa del sistema del complemento.
La opsonización es el proceso por el cual moléculas como C3b se depositan sobre la superficie de los patógenos, marcándolos para ser reconocidos y fagocitados por células del sistema inmunitario como macrófagos y neutrófilos. Estos fagocitos poseen receptores específicos (CR1, CR3, CR4) que reconocen los fragmentos de C3b, facilitando enormemente la captura e ingestión de los microorganismos. Es una de las funciones más importantes del complemento.
Las anafilotoxinas son fragmentos pequeños (C3a, C4a y C5a) liberados durante la activación del complemento que actúan como potentes mediadores de la inflamación. C5a es la más potente y actúa como quimioatrayente de neutrófilos, activador de macrófagos y promotor del aumento de la permeabilidad vascular. Estas moléculas también estimulan la degranulación de mastocitos y la liberación de histamina, contribuyendo a la respuesta inflamatoria local.
Las células del organismo poseen múltiples proteínas reguladoras que impiden la activación del complemento en sus superficies. Entre ellas destacan DAF (CD55), que disocia las convertasas; MCP (CD46), que facilita la degradación de C3b; y CD59, que impide la formación del MAC. Además, el factor H se une preferentemente a C3b en células propias gracias al ácido siálico de sus membranas, promoviendo su inactivación. La ausencia de estos reguladores en los patógenos permite la activación selectiva del complemento.
Las deficiencias del complemento se asocian con diversas patologías según el componente afectado. La deficiencia de C3 causa infecciones bacterianas graves y recurrentes. La deficiencia de componentes terminales (C5-C9) predispone a infecciones por Neisseria meningitidis. La deficiencia de C1 inhibidor causa angioedema hereditario. La deficiencia de MBL aumenta las infecciones en la primera infancia. Las mutaciones en CD59 y DAF causan hemoglobinuria paroxística nocturna con destrucción de glóbulos rojos propios.
La principal diferencia radica en su mecanismo de activación. La vía clásica requiere la presencia de anticuerpos unidos al patógeno para activarse, ya que C1q reconoce las regiones Fc de IgG e IgM, conectando la inmunidad adaptativa con el complemento. La vía alternativa, en cambio, se activa de forma espontánea e independiente de anticuerpos mediante la hidrólisis continua de C3 en el plasma, proporcionando una defensa inmediata desde el primer contacto con el patógeno. Ambas vías generan C3 convertasas diferentes pero convergen en la misma cascada terminal.