¿Qué son los macrófagos?
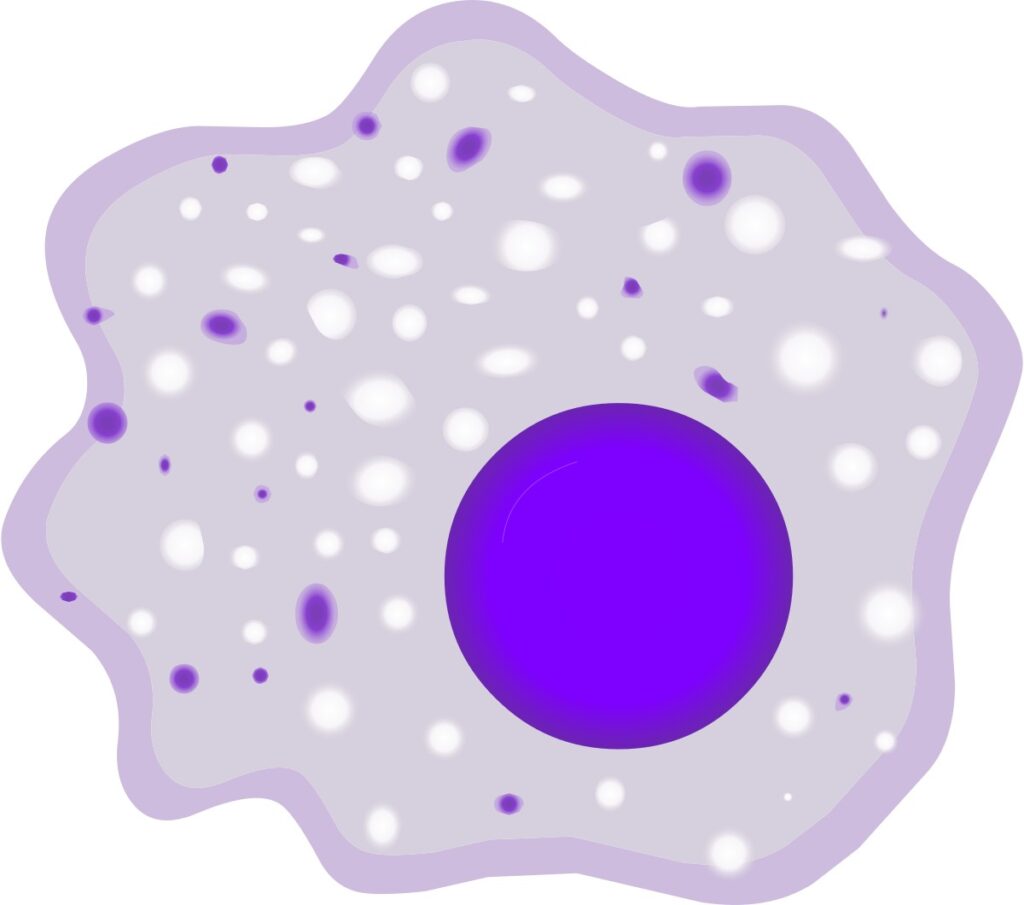
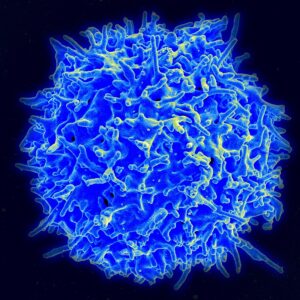
Los macrófagos son un tipo de glóbulo blanco (leucocito) que pertenece al grupo de los fagocitos, células especializadas en ingerir y digerir microorganismos, partículas extrañas y restos celulares. Son células grandes, con un diámetro de entre 15 y 25 micrómetros, dotadas de una gran capacidad para desplazarse a través de los tejidos gracias a la emisión de prolongaciones citoplasmáticas llamadas pseudópodos.
Estas células forman parte del sistema fagocítico mononuclear y constituyen una de las primeras líneas de defensa del organismo. A diferencia de los linfocitos, que actúan de forma específica contra un antígeno concreto, los macrófagos poseen una capacidad de reconocimiento amplia gracias a los receptores de reconocimiento de patrones (PRR), como los receptores tipo Toll (TLR), que identifican moléculas comunes a muchos patógenos conocidas como patrones moleculares asociados a patógenos (PAMP).
Además de su función defensiva, los macrófagos participan en procesos de homeostasis tisular, eliminando células apoptóticas (muertas por muerte celular programada) y contribuyendo a la remodelación de tejidos durante el desarrollo embrionario, la cicatrización de heridas y la resolución de la inflamación.
Origen de los macrófagos: de monocitos a macrófagos
La mayoría de los macrófagos se originan a partir de los monocitos, un tipo de leucocito producido en la médula ósea mediante un proceso denominado hematopoyesis. Los monocitos se liberan al torrente sanguíneo, donde circulan durante aproximadamente 1 a 3 días antes de migrar hacia los tejidos en respuesta a señales químicas de inflamación o daño tisular.
Una vez que los monocitos abandonan los vasos sanguíneos mediante un proceso llamado diapédesis (atravesando la pared de los capilares), experimentan una serie de cambios morfológicos y funcionales que los transforman en macrófagos maduros. Este proceso de diferenciación incluye:
- Aumento significativo del tamaño celular.
- Incremento del número de lisosomas, orgánulos que contienen enzimas digestivas.
- Mayor producción de receptores de superficie para reconocer patógenos.
- Desarrollo de una mayor capacidad fagocítica y de producción de citocinas.
Sin embargo, investigaciones recientes han demostrado que no todos los macrófagos provienen de monocitos circulantes. Algunos macrófagos residentes en tejidos, como la microglía del cerebro y las células de Kupffer del hígado, se originan durante el desarrollo embrionario a partir de precursores del saco vitelino y el hígado fetal, y se mantienen en los tejidos durante toda la vida mediante autorrenovación local.
Tipos de macrófagos
Dependiendo del tejido donde residen, los macrófagos reciben diferentes nombres y adquieren funciones especializadas. Los principales tipos son:
Macrófagos alveolares
Se encuentran en los alvéolos pulmonares y constituyen la primera línea de defensa contra los patógenos inhalados. Son responsables de eliminar partículas de polvo, bacterias, esporas de hongos y otros contaminantes que llegan a los pulmones con cada respiración. También desempeñan un papel importante en la regulación de la respuesta inflamatoria pulmonar y en el mantenimiento del surfactante pulmonar.
Células de Kupffer
Son los macrófagos residentes del hígado, localizados en los sinusoides hepáticos. Representan aproximadamente el 80-90% de los macrófagos tisulares del cuerpo. Su función principal es filtrar la sangre que llega del intestino a través de la vena porta, eliminando bacterias, endotoxinas, complejos inmunitarios y eritrocitos envejecidos. También participan en el metabolismo del hierro y la bilirrubina.
Microglía
Son los macrófagos residentes del sistema nervioso central (cerebro y médula espinal). La microglía vigila constantemente el entorno cerebral en busca de daños, infecciones o acumulación de proteínas anormales. Desempeña funciones cruciales en la poda sináptica durante el desarrollo neuronal, la eliminación de neuronas dañadas y la respuesta a lesiones cerebrales. Su activación excesiva se ha asociado con enfermedades neurodegenerativas como el Alzheimer y el Parkinson.
Osteoclastos
Son células multinucleadas derivadas de la fusión de precursores monocíticos que se encargan de la resorción ósea. Los osteoclastos degradan la matriz ósea mineralizada liberando calcio y fósforo al torrente sanguíneo, un proceso esencial para la remodelación continua del esqueleto y la homeostasis mineral. Un desequilibrio en la actividad osteoclástica puede conducir a enfermedades como la osteoporosis (exceso de resorción) o la osteopetrosis (resorción insuficiente).
Otros tipos de macrófagos tisulares incluyen los histiocitos del tejido conectivo, los macrófagos peritoneales de la cavidad abdominal, los macrófagos esplénicos del bazo y los macrófagos de la médula ósea.
Fagocitosis: cómo los macrófagos destruyen patógenos
La fagocitosis es el proceso central mediante el cual los macrófagos eliminan microorganismos y partículas extrañas. Este mecanismo se desarrolla en varias etapas bien definidas:
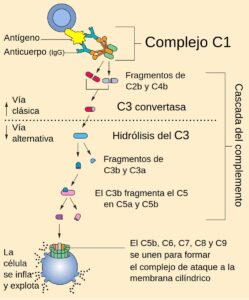
- Quimiotaxis: los macrófagos son atraídos hacia el sitio de infección o daño tisular por señales químicas como quimiocinas, componentes del complemento (C3a y C5a) y productos bacterianos.
- Reconocimiento y adhesión: los receptores de superficie del macrófago (receptores tipo Toll, receptores de manosa, receptores scavenger) reconocen y se unen a las moléculas de la superficie del patógeno. La opsonización, es decir, el recubrimiento del patógeno con anticuerpos (IgG) o proteínas del complemento (C3b), facilita enormemente este reconocimiento.
- Ingestión: el macrófago extiende sus pseudópodos alrededor del patógeno y lo envuelve formando una vesícula intracelular denominada fagosoma.
- Digestión: el fagosoma se fusiona con los lisosomas para formar el fagolisosoma, donde el patógeno es destruido mediante enzimas hidrolíticas (proteasas, lipasas, nucleasas), especies reactivas de oxígeno (estallido respiratorio), óxido nítrico y un pH ácido de aproximadamente 4,5.
- Eliminación: los restos digeridos del patógeno son expulsados de la célula por exocitosis o reciclados para la presentación de antígenos.
Un solo macrófago puede fagocitar y destruir más de 100 bacterias a lo largo de su vida, que puede extenderse durante meses o incluso años en los tejidos.
Función como presentadores de antígenos
Además de destruir patógenos, los macrófagos desempeñan un papel crítico como células presentadoras de antígenos (CPA), sirviendo de puente entre la inmunidad innata y la inmunidad adaptativa. Tras digerir un microorganismo, los macrófagos procesan sus proteínas y presentan fragmentos de estas (péptidos antigénicos) en su superficie celular unidos a moléculas del complejo mayor de histocompatibilidad de clase II (MHC-II).
Estos complejos péptido-MHC-II son reconocidos por los linfocitos T colaboradores (CD4+), lo que desencadena una cascada de respuestas inmunitarias adaptativas que incluyen:
- Activación y proliferación de linfocitos T específicos contra el patógeno.
- Estimulación de linfocitos B para producir anticuerpos.
- Generación de células de memoria inmunológica para una respuesta más rápida en futuras infecciones.
Los macrófagos también secretan citocinas como la interleucina-1 (IL-1), la interleucina-12 (IL-12) y el factor de necrosis tumoral alfa (TNF-α), que activan y dirigen la respuesta de los linfocitos. De esta manera, los macrófagos no solo eliminan amenazas de forma directa, sino que también instruyen al sistema inmunitario adaptativo sobre qué patógenos debe combatir.
Papel en la inflamación
Los macrófagos son actores centrales en el proceso inflamatorio, participando tanto en su inicio como en su resolución. Según su estado de activación, los macrófagos pueden clasificarse en dos fenotipos principales:
Macrófagos M1 (activación clásica)
Son activados por señales proinflamatorias como el interferón gamma (IFN-γ) y los lipopolisacáridos bacterianos (LPS). Los macrófagos M1 producen grandes cantidades de citocinas proinflamatorias (TNF-α, IL-1β, IL-6, IL-12), especies reactivas de oxígeno y óxido nítrico. Su función principal es la eliminación de patógenos y la activación de la respuesta inmunitaria. Predominan en las fases iniciales de la inflamación.
Macrófagos M2 (activación alternativa)
Son inducidos por citocinas antiinflamatorias como la interleucina-4 (IL-4) e interleucina-13 (IL-13). Los macrófagos M2 producen citocinas antiinflamatorias (IL-10, TGF-β) y factores de crecimiento que promueven la reparación tisular, la angiogénesis (formación de nuevos vasos sanguíneos) y la resolución de la inflamación. Predominan en las fases tardías del proceso inflamatorio.
El equilibrio entre los fenotipos M1 y M2 es fundamental para una respuesta inmunitaria adecuada. Una activación M1 prolongada puede causar daño tisular crónico, mientras que una polarización excesiva hacia M2 puede facilitar la evasión de patógenos o el crecimiento tumoral.
Macrófagos y enfermedades
La disfunción de los macrófagos está implicada en numerosas enfermedades, tanto por defecto como por exceso de actividad:
Aterosclerosis
Los macrófagos que infiltran la pared arterial fagocitan lipoproteínas de baja densidad oxidadas (LDL oxidadas), transformándose en células espumosas cargadas de colesterol. La acumulación de estas células espumosas contribuye a la formación de la placa aterosclerótica, que puede estrechar las arterias y provocar infartos de miocardio o accidentes cerebrovasculares.
Enfermedades autoinmunes
En enfermedades como la artritis reumatoide, la enfermedad inflamatoria intestinal y el lupus eritematoso sistémico, los macrófagos contribuyen al daño tisular mediante la producción excesiva de citocinas proinflamatorias y la destrucción de tejidos propios del organismo.
Cáncer
Los macrófagos asociados a tumores (TAM) suelen adoptar un fenotipo M2 que promueve el crecimiento tumoral, la angiogénesis, la supresión de la respuesta inmunitaria antitumoral y la metástasis. Por esta razón, la reprogramación de los TAM hacia un fenotipo M1 antitumoral es una estrategia prometedora en la inmunoterapia del cáncer.
Enfermedades infecciosas
Algunos patógenos han desarrollado mecanismos para sobrevivir dentro de los macrófagos, como Mycobacterium tuberculosis (tuberculosis), Leishmania y el VIH, que utiliza los macrófagos como reservorios virales. La incapacidad de los macrófagos para destruir estos patógenos intracelulares puede llevar a infecciones crónicas o granulomatosas.
Enfermedades neurodegenerativas
La activación crónica de la microglía se ha vinculado con la progresión de enfermedades como el Alzheimer, el Parkinson y la esclerosis lateral amiotrófica (ELA). La neuroinflamación sostenida mediada por la microglía contribuye a la muerte neuronal y al deterioro cognitivo progresivo.
Los macrófagos son un tipo de glóbulo blanco del sistema inmunitario innato cuya función principal es fagocitar (engullir y destruir) bacterias, virus, hongos, células dañadas y sustancias extrañas. También actúan como células presentadoras de antígenos, activando la respuesta inmunitaria adaptativa, y participan en la reparación de tejidos y la regulación de la inflamación.
Los monocitos son células precursoras que circulan en la sangre, producidas en la médula ósea. Cuando migran desde el torrente sanguíneo hacia los tejidos en respuesta a señales de inflamación, se diferencian y maduran convirtiéndose en macrófagos, que son más grandes, tienen más lisosomas y poseen una mayor capacidad fagocítica y de producción de citocinas.
La fagocitosis es el proceso por el cual los macrófagos engullen y destruyen patógenos y partículas extrañas. Consta de varias etapas: primero el macrófago es atraído por señales químicas (quimiotaxis), luego reconoce al patógeno mediante receptores de superficie, lo envuelve con pseudópodos formando un fagosoma, que se fusiona con lisosomas para destruir el patógeno mediante enzimas y sustancias tóxicas.
Existen varios tipos según el tejido donde residen: macrófagos alveolares en los pulmones, células de Kupffer en el hígado, microglía en el sistema nervioso central, osteoclastos en los huesos, histiocitos en el tejido conectivo, macrófagos peritoneales en la cavidad abdominal y macrófagos esplénicos en el bazo. Cada tipo tiene funciones especializadas adaptadas a su localización.
Los macrófagos M1 (activación clásica) son proinflamatorios, producen citocinas como TNF-α e IL-6, y se especializan en destruir patógenos. Los macrófagos M2 (activación alternativa) son antiinflamatorios, producen IL-10 y TGF-β, y promueven la reparación tisular y la resolución de la inflamación. El equilibrio entre ambos fenotipos es esencial para una respuesta inmunitaria adecuada.
Tras fagocitar y digerir un patógeno, los macrófagos procesan sus proteínas y presentan fragmentos peptídicos en su superficie unidos a moléculas MHC de clase II. Los linfocitos T colaboradores (CD4+) reconocen estos complejos, lo que activa la respuesta inmunitaria adaptativa, incluyendo la producción de anticuerpos por linfocitos B y la generación de células de memoria inmunológica.
Los macrófagos están implicados en numerosas enfermedades: aterosclerosis (por formación de células espumosas), enfermedades autoinmunes como artritis reumatoide y lupus, cáncer (los macrófagos asociados a tumores pueden promover el crecimiento tumoral), infecciones crónicas como tuberculosis y VIH, y enfermedades neurodegenerativas como Alzheimer y Parkinson por activación excesiva de la microglía.
Sí. Mantener un sistema inmunitario saludable mediante una alimentación equilibrada rica en vitaminas C, D y zinc, ejercicio moderado regular, sueño adecuado y manejo del estrés favorece el funcionamiento óptimo de los macrófagos. Además, en el ámbito clínico se investigan terapias de inmunomodulación que buscan reprogramar macrófagos para combatir el cáncer y enfermedades infecciosas crónicas.