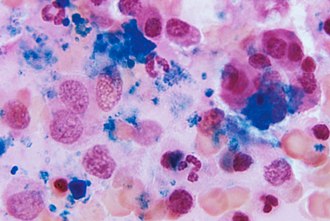
Médula roja y médula amarilla
- Médula roja: activa hematopoyéticamente. En adultos se limita a esternón, vértebras, costillas, pelvis y epífisis proximales del fémur y húmero.
- Médula amarilla: rica en adipocitos, sin actividad hematopoyética normal. Puede reactivarse en anemias graves.
Hematopoyesis
Todas las células sanguíneas derivan de la célula madre hematopoyética pluripotente (HSC). A través de cascadas de diferenciación reguladas por factores de crecimiento (eritropoyetina, trombopoyetina, G-CSF), se producen eritrocitos, leucocitos y plaquetas. El proceso tarda 7-14 días desde la HSC hasta la célula madura.
Trasplante de médula ósea
El trasplante de células madre hematopoyéticas es el tratamiento de elección para leucemias, linfomas, mielomas y anemias aplásicas graves. Puede ser alogénico (donante compatible HLA) o autólogo (células del propio paciente). La principal complicación del alogénico es la enfermedad injerto contra huésped (EICH).
Estructura microscópica y microambiente medular
La médula ósea roja tiene una organización histológica muy precisa. Las células hematopoyéticas se distribuyen en nichos o compartimentos especializados del estroma medular: el nicho endosteal, cerca del hueso, alberga las células madre más quiescentes; el nicho vascular, alrededor de los sinusoides, es donde ocurre la maduración celular y la liberación de células al torrente sanguíneo. El estroma está formado por células reticulares, fibroblastos, células endoteliales, osteoblastos y adipocitos, que forman una red de sostén y secretan factores de crecimiento indispensables para la hematopoyesis.
Las células madre hematopoyéticas (HSC) representan apenas 1 de cada 10.000 células medulares. Son capaces de autorrenovarse (producir más HSC) y diferenciarse hacia dos grandes linajes: el mieloide (eritrocitos, plaquetas, granulocitos, monocitos) y el linfoide (linfocitos B, T y células NK). Esta plasticidad es la base del trasplante de médula ósea: un pequeño número de HSC es suficiente para repoblar toda la médula de un receptor.
Regulación de la hematopoyesis
La producción de células sanguíneas está finamente regulada por factores de crecimiento hematopoyéticos. La eritropoyetina (EPO), producida por el riñón en respuesta a la hipoxia, estimula la producción de glóbulos rojos. La trombopoyetina (TPO), sintetizada principalmente en el hígado, regula la megacariopoyesis y la producción de plaquetas. El factor estimulante de colonias de granulocitos (G-CSF) incrementa la producción de neutrófilos y es usado clínicamente para tratar la neutropenia severa. La interleucina-3 (IL-3) actúa sobre múltiples linajes como factor de crecimiento multilinaje.
Durante la vida fetal, la hematopoyesis ocurre en el saco vitelino (semanas 3-8), el hígado y el bazo (semanas 6-28) y finalmente en la médula ósea a partir del quinto mes. Al nacer, toda la médula es roja y activa. Con el crecimiento, la médula de los huesos largos se convierte progresivamente en médula amarilla hasta que en la edad adulta solo persiste médula roja en los huesos axiales. En situaciones de demanda extrema, como en las anemias hemolíticas crónicas, la médula amarilla puede reconvertirse a roja, y el hígado y el bazo pueden retomar su función hematopoyética (hematopoyesis extramedular).
Enfermedades relacionadas con la médula ósea
- Leucemia: proliferación maligna de células hematopoyéticas en la médula; puede ser aguda (mieloide o linfoide) o crónica; es la indicación más frecuente de trasplante alogénico.
- Anemia aplásica: fallo medular grave con pancitopenia por destrucción o ausencia de células madre; puede ser idiopática, tóxica o autoinmune; se trata con trasplante alogénico o inmunosupresión.
- Mieloma múltiple: neoplasia de células plasmáticas que infiltra la médula ósea, produce inmunoglobulinas monoclonales y causa destrucción ósea, anemia e insuficiencia renal.
- Síndrome mielodisplásico: grupo de trastornos por hematopoyesis ineficaz con citopenias periféricas; mayor riesgo de transformación a leucemia aguda mieloide.
- Mielofibrosis: sustitución del tejido hematopoyético por fibrosis colágena; causa anemia, esplenomegalia masiva por hematopoyesis extramedular y síntomas constitucionales.
- Metástasis óseas medulares: frecuentes en cánceres de mama, próstata, pulmón y riñón; pueden causar pancitopenia por invasión de la médula (mieloptisis) y fracturas patológicas.
En el trasplante alogénico, las células madre proceden de un donante compatible (familiar HLA-idéntico o donante no emparentado del registro). Ofrece el beneficio del efecto injerto contra leucemia, pero conlleva el riesgo de enfermedad injerto contra huésped (EICH), potencialmente grave. En el trasplante autólogo, se usan las propias células del paciente, previamente recolectadas y criopreservadas; no hay riesgo de EICH pero tampoco efecto antitumoral del injerto. Se emplea principalmente en mieloma múltiple y linfomas.
Existen tres fuentes principales: la aspiración directa de médula ósea de la cresta ilíaca bajo anestesia general, la movilización y recolección de células madre de la sangre periférica mediante aféresis tras estimulación con G-CSF (método más usado actualmente), y la sangre de cordón umbilical, que se conserva en bancos especializados. La sangre periférica movilizada es la fuente preferida por su menor invasividad y mayor velocidad de injerto.
La biopsia de médula ósea (BMO) permite analizar la celularidad, arquitectura y presencia de células anormales en la médula. Es fundamental para diagnosticar leucemias, linfomas, mieloma, anemia aplásica, mielodisplasias y metástasis. Se realiza habitualmente bajo anestesia local en la cresta ilíaca posterosuperior, extrayendo un cilindro de hueso con una aguja de Jamshidi. El procedimiento dura 10-15 minutos y es ambulatorio.
Depende del grado de daño. Tras quimioterapia convencional, la médula se recupera sola en 2-4 semanas. Tras quimioterapia de alta dosis o irradiación corporal total, la médula queda destruida de forma irreversible y requiere un trasplante de células madre para regenerarse. En la anemia aplásica grave de causa autoinmune, el tratamiento inmunosupresor (globulina antitimocítica más ciclosporina) puede rescatar suficiente función medular residual en pacientes sin donante compatible.